晚期胃肠间质瘤新药获批上市
2021年3月31日,国家药品监督管理局批准了擎乐®(瑞派替尼)的新药上市申请(NDA),用于治疗已接受过包括伊马替尼在内的3种及以上激酶抑制剂治疗的晚期胃肠间质瘤成人患者。擎乐®可广泛抑制KIT和PDGFRα导致的GIST的突变激酶。4月17日,该药于海南海口上市,胃肠肿瘤高峰论坛同日举行,600余位胃肠肿瘤领域的专家与临床医生汇聚一堂,围绕胃肠肿瘤的诊疗现状与发展趋势展开深入交流。

得益于“国九条”等优惠政策,擎乐®在全球首次获批后仅2个月就进入海南乐城先行区惠及中国患者,并创下三个“首个”:乐城先行区首个与全球患者同步使用的新药、首个特批带离先行区使用的临床急需药品,首个落地的离岛患者管理项目。随着今年国家药品监督管理局批准了擎乐®用于晚期胃肠间质瘤治疗上市申请,这款创新药物正式从海南走向全国。
胃肠间质瘤(GIST)是发病率仅次于胃癌和结直肠癌的消化道肿瘤,中国每年约有3万名新诊断患者,是美国和欧洲新诊断患者之和的两倍,估计超过10万名正在进行治疗的胃肠间质瘤患者,而恶性胃肠间质瘤也被认为是最难以治疗的肿瘤之一。
中国临床肿瘤学会(CSCO)胃肠间质瘤专家委员会主任委员,北京大学人民医院胃肠外科主任叶颖江教授介绍,GIST的治疗过程中面临着很多挑战,大部分的胃肠间质瘤由一系列突变驱动,其中最常见原发突变的为KIT激酶突变和PDGFRα激酶突变。晚期、转移的GIST患者在一线治疗后,大都会出现耐药情况。在瑞派替尼出现之前,三线治疗之后的GIST患者由于过往治疗手段无法抑制造成耐药及疾病进展的原发和继发突变,缺乏有效治疗方式。
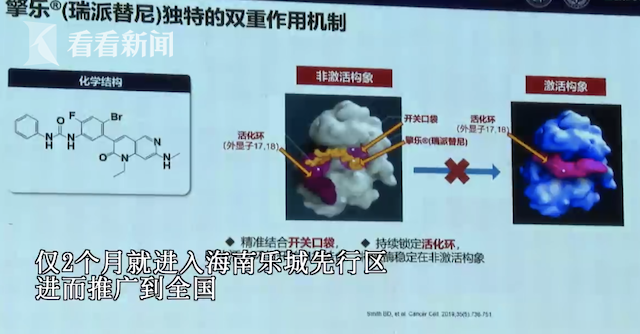
擎乐®作为中国大陆首个获批上市的GIST四线治疗药物,填补了中国患者在这一疾病治疗领域的空白。中国医师协会外科分会GIST诊疗专委会主任委员,上海交通大学医学院附属仁济医院外科主任、胃肠外科主任曹晖教授介绍道,擎乐®是具有崭新机制的“开关控制”抑制剂,一天一次口服,并且无需基因检测,这对GIST患者来说是一个重要的里程碑。

再鼎医药创始人、董事长兼首席执行官杜莹博士在致辞中表示,由于缺乏有效的后线药物,患者在治疗上存在着巨大的未满足需求。国家药监局对擎乐®的批准将为中国四线GIST患者建立起全新的标准治疗。
海南省抗癌协会理事长,海南省人民医院胃肠外科周卫平教授介绍,擎乐®于去年7月正式落地博鳌乐城先行区并惠及首位患者后,目前已经累计惠及约20名患者。
在本次论坛上,中华慈善总会还启动了“爱无间——GIST患者全程关爱社区”公益项目。该项目旨在通过数字化手段,对胃肠间质瘤患者进行线上线下的患教科普,由医生对患者进行疾病全程管理,帮助患者进行规范化治疗,从而获得更好的生存获益。
(看看新闻Knews记者:敖德芳 符雅 王则斌 实习编辑:骆惠)
推荐视频

剑网行动举报电话:12318(市文化执法总队)、021-64334547(市版权局)
Copyright © 2016 Kankanews.com Inc. All Rights Reserved. 看东方(上海)传媒有限公司 版权所有

























 沪公网安备 31010602001114号
沪公网安备 31010602001114号
全部评论
暂无评论,快来发表你的评论吧